Soient les différentielle totales
1) Expliciter les relations imposées par le fait que
On s’intéresse à l’équation d’état
2) Calculer
3) On s’intéresse successivement aux équations d’état
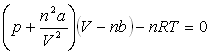 .
.Reprendre la question 2 avec les mêmes hypothèses.
Exercices sur la recherche des fonctions d'état et l'étude des quatre transformations de base (adiabatique, isotherme, isochore, isobare)
Méthodologie commune aux exercices ci-après
1 - Les variables d’état pression p, volume V et
température T sont reliées par une équation de type
f(p,V,T)=0 appelée équation d’état. On peut aussi
écrire l’équation d’état, par exemple sous la forme p=p(V,T)
où la variable d’état p apparaît alors comme une
fonction des variables indépendantes V et T.
Soient les différentielle totales ![]() et
et ![]() où
où ![]() et
et ![]() sont les coefficients
calorimétriques qui dépendent des variables d’état.
sont les coefficients
calorimétriques qui dépendent des variables d’état.
1) Expliciter les relations imposées par le fait que ![]() et
et ![]() sont des différentielles
totales.
sont des différentielles
totales.
On s’intéresse à l’équation d’état ![]() où
où ![]() et
et ![]() sont des constantes.
sont des constantes.
2) Calculer ![]() ;
montrer que
;
montrer que ![]() ne
dépend pas de
ne
dépend pas de ![]() ,
calculer les fonctions d’état
,
calculer les fonctions d’état ![]() et
et ![]() en supposant
que
en supposant
que ![]() ne dépend
pas de
ne dépend
pas de ![]() .
.
3) On s’intéresse successivement aux équations d’état ![]() et
et 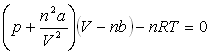 .
.
Reprendre la question 2 avec les mêmes hypothèses.
| Réponse 1) | Réponse 2) | Réponse 3)a) | Réponse 3)b) |
2 - Les variables d’état pression p, volume V
et température T sont reliées par une équation de
type f(p,V,T)=0 appelée équation d’état. On peut
aussi écrire l’équation d’état, par exemple sous la forme
V=V(p,T) où la variable d’état V apparaît
alors comme une fonction des variables indépendantes p et T.
Soient les différentielles totales : ![]() et
et ![]() où
où ![]() et
et
![]() sont les coefficients
calorimétriques qui dépendent des valeurs des variables d’état.
sont les coefficients
calorimétriques qui dépendent des valeurs des variables d’état.
1) Expliciter les relations imposées par le fait que ![]() et
et ![]() sont des différentielles
totales.
sont des différentielles
totales.
On s’intéresse à l’équation d’état ![]() où
où ![]() et
et ![]() sont des constantes.
sont des constantes.
2) Calculer ![]() ;
montrer que
;
montrer que ![]() ne
dépend pas de
ne
dépend pas de ![]() ,
calculer les fonctions d’état
,
calculer les fonctions d’état ![]() et
et ![]() en supposant
que
en supposant
que ![]() ne dépend
pas de
ne dépend
pas de ![]() .
.
3) Reprendre la questions 2) avec les mêmes hypothèses et l’équation
d’état ![]() où
où ![]() ,
, ![]() ,
,
![]() et
et ![]() sont des constantes.
sont des constantes.
| Réponse 1) | Réponse 2) | Réponse 3) |
-------------------------------------------------------------------------------------------
Méthodologie commune aux exercices ci-après
Les exercices 3, 4, 5 et 6 ont pour objet d'étudier les quatre transformations (adiabatique, isotherme, isochore et isobare) et les raisonnements à tenir. Pour le corps envisagé, les fonctions d'état U, H et S sont connues. Elles ont pu être calculées à partir de la connaissance de l'équation d'état et d'une donnée sur la capacité calorifique à volume constant (pour calculer U et en déduire H) ou à pression constante (pour calculer H et en déduire U) comme il a été montré dans les exercices 1 et 2.
3 - On étudie la compression adiabatique de la
pression ![]() à
la pression
à
la pression ![]() d’un
corps initialement à la température
d’un
corps initialement à la température ![]() et de volume
et de volume ![]() .
.
1) Dans le cas d’une transformation réversible, calculer ![]() et
et ![]() ; calculer le
travail W échangé et l’entropie
; calculer le
travail W échangé et l’entropie ![]() créée.
créée.
2) Dans le cas d’une transformation irréversible (la pression extérieure
est ![]() ), calculer
), calculer
![]() et
et ![]() ;
calculer le travail W’ échangé et l’entropie
;
calculer le travail W’ échangé et l’entropie ![]() créée.
créée.
3) Comparer W et W’ d’une part, ![]() et
et ![]() d’autre part.
d’autre part.
| Réponse 1) | Réponse 2) | Réponse 3) |
4 - On étudie la compression isotherme à
la température ![]() de la pression
de la pression ![]() à la pression
à la pression ![]() d’un corps initialement de volume
d’un corps initialement de volume ![]() .
.
1) Calculer le volume final ![]() .
.
2) Dans le cas d’une transformation réversible, calculer la chaleur Q
et le travail W échangés, l’entropie ![]() créée.
créée.
3) Dans le cas d’une transformation irréversible (la pression extérieure
étant ![]() ),
calculer la chaleur Q’ et le travail W’ échangés,
l’entropie
),
calculer la chaleur Q’ et le travail W’ échangés,
l’entropie ![]() créée.
créée.
4) Comparer W et W’ d’une part, Q et Q’ d’autre
part.
| Réponse 1) | Réponse 2) | Réponse 3) | Réponse 4) |
5 - On étudie la transformation isochore à
volume ![]() de la pression
de la pression
![]() à la pression
à la pression
![]() d’un corps initialement
à température
d’un corps initialement
à température ![]() .
.
1) Calculer la température finale![]() .
.
2) Dans le cas d’une transformation réversible, calculer la chaleur Q,
l’entropie ![]() créée.
créée.
3) Dans le cas d’une transformation irréversible (le corps est mis en
contact avec une source à température ![]() ),
calculer la chaleur Q’, l’entropie
),
calculer la chaleur Q’, l’entropie ![]() créée.
créée.
| Réponse 1) | Réponse 2) | Réponse 3) |
6 - On étudie la transformation isobare à
pression ![]() de la
température
de la
température ![]() à la température
à la température ![]() d’un corps initialement au volume
d’un corps initialement au volume ![]() .
.
1) Calculer le volume final ![]() .
.
2) Dans le cas d’une transformation réversible, calculer la chaleur Q
et le travail W, l’entropie ![]() créée.
créée.
3) Dans le cas d’une transformation irréversible (le corps est mis en
contact avec une source à température ![]() ),
calculer la chaleur Q’ et le travail W’, l’entropie
),
calculer la chaleur Q’ et le travail W’, l’entropie ![]() créée.
créée.
| Réponse 1) | Réponse 2) | Réponse 3) |