Chapitre 4 : Transferts dénergie et bilans
énergétiques
Nous limitons nos propos aux variables détat pression, volume,
température et quantité de matière.
1. Variables intensives et extensives
Nous considérons un système Shomogène,
sous une seule phase, en équilibre. Les variables détat
y sont uniformes et constantes.
Elles sont liées par une équation détat f(p,
V, T, n ou m) = 0.
Considérons une partie S de S
et notons que dans cette partie pression p et température
T
sont inchangées alors que le volume est devenu lV,
la quantité de matière ln
ou lm où l
est compris entre 0 et 1.
Les variables détat ont un caractère différent.
On dira que pression et température sont des variables intensives,
que volume et quantité de matière sont des variables
extensives.
Ainsi si nous écrivons léquation détat pour
S
sous la forme V = V(T, p, n ou m), elle sécrira pour S
lV=
V(T, p, ln ou lm)
cest à dire que la fonction
V est une fonction homogène
de degré 1 en n ou en m.
La notation générale que nous utilisons est la suivante
:
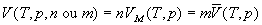
Lindice M indique quune quantité est rapportée
à une mole de matière (on dit molaire), la barre  quelle est rapportée à lunité de masse de matière
(on dit massique).
quelle est rapportée à lunité de masse de matière
(on dit massique).
Nous avons noté le caractère additif des fonctions
détat U et S ; pour un système homogène,
sous une phase, en équilibre ces fonctions seront extensives.
Il en sera, de même, de la fonction détat enthalpie H
= U + pV , la quantité pV produit dune variable intensive
par une variable extensive étant extensive.
2. Travail des forces de pression extérieure
Le piston (paroi mobile en translation) est la technologie la plus
simple pour aborder léchange dénergie par travail provoquant
un changement de létat interne du système. Les études
de technologies liées à des roues mobiles (turbines) sont
plus complexes et ne sont pas envisagées dans le cadre du DEUG A.
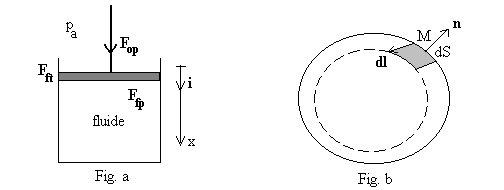
Fig. a - Nous raisonnons sur un piston plan de section S dont
le déplacement est suivant la direction verticale x. Ce cas particulier
nenlève rien à la généralité de nos propos.
Il est soumis à la force de lopérateur extérieur de composante
verticale 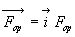 ,
à son poids
,
à son poids 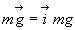 ,
à la pression de lenvironnement
,
à la pression de lenvironnement 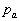 ,
à la force tangentielle de frottement de contact
,
à la force tangentielle de frottement de contact 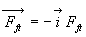 (seule la projection tangentielle travaille) et à la force
(seule la projection tangentielle travaille) et à la force 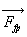 quexerce le système fluide sur le piston (
quexerce le système fluide sur le piston (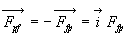 est la force exercée par le piston sur le fluide).
est la force exercée par le piston sur le fluide).
Nous cherchons à connaître le travail dW
échangé par le système fluide du à laction du piston,
soit 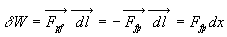 où
où 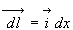 est le vecteur déplacement élémentaire du piston.
est le vecteur déplacement élémentaire du piston.
Lapplication du théorème de lénergie cinétique
au piston permet décrire :
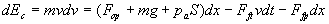
Pour le travail de la force de frottement, la vitesse à considérer
est celle de glissement du piston sur la paroi du cylindre qui, ici , se
confond avec la vitesse v du piston puisque le mouvement est une translation.
La pression extérieure est définie par la relation 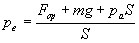 si bien que le travail échangé sécrit
si bien que le travail échangé sécrit 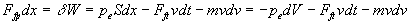 où nous avons introduit
où nous avons introduit 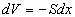 variation de volume du système fluide (pour un déplacement du
piston positif, nous avons une diminution de volume du système ce qui
explique lorigine du signe moins).
variation de volume du système fluide (pour un déplacement du
piston positif, nous avons une diminution de volume du système ce qui
explique lorigine du signe moins).
Lexpression de dW est, même
pour ce cas simplifié, difficilement manipulable car il nous faut
connaître le problème mécanique.
Aussi nous envisageons dW,
- pour un travail des forces de frottement négligeable (le but
étant déchanger du travail avec le système fluide,
les parties mécaniques piston-paroi sont lubrifiées et la
vitesse de glissement est suffisamment faible),
- pour une énergie cinétique négligeable (vitesse
de déplacement du piston suffisamment faible et/ou masse du piston
négligeable)
alors le travail échangé est égal à 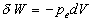
Fig. b - Dans le cas général, le calcul doit être
fait à chaque élément de surface dS sans faire
dhypothèse sur les directions des forces ou des déplacements.
La pression extérieure 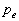 au
point M doit être comprise comme la somme de la pression denvironnement
au
point M doit être comprise comme la somme de la pression denvironnement  et des projections, suivant la normale à lélément de surface,
des forces extérieures (force dopérateur et poids).
et des projections, suivant la normale à lélément de surface,
des forces extérieures (force dopérateur et poids).
Alors 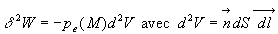 (en
négligeant le travail des forces de frottement de contact et lénergie
cinétique de lélément de surface)
(en
négligeant le travail des forces de frottement de contact et lénergie
cinétique de lélément de surface)
Remarque : si 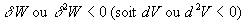 ,
le travail est moteur (le système " pousse " sur le milieu extérieur)
; il est récepteur dans le cas opposé.
,
le travail est moteur (le système " pousse " sur le milieu extérieur)
; il est récepteur dans le cas opposé.
Cas dune pression extérieure uniforme
Dans ce cas là, entre deux instants successifs, nous pouvons intégrer
lexpression de 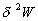 à tous les éléments de surface.
à tous les éléments de surface.
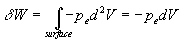 où dV
est la variation de volume du système.
où dV
est la variation de volume du système.
Cas dune transformation quasistatique, dune transformation réversible
Le système est en état déquilibre ou très
voisin dun état déquilibre. Les vitesses de déplacement
ou de glissement sont " nulles ".
La pression du système est uniforme et égale à
p.
En écrivant le principe fondamental de la dynamique sur chaque élément
de surface, on obtient :
* 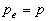 (transformation
réversible ; cette condition traduit aussi la condition déquilibre
mécanique sur une paroi mobile)
(transformation
réversible ; cette condition traduit aussi la condition déquilibre
mécanique sur une paroi mobile)
* 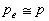 (transformation
quasistatique).
(transformation
quasistatique).
Le travail échangé est égal à 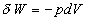
Représentation du travail dans un diagramme V, p
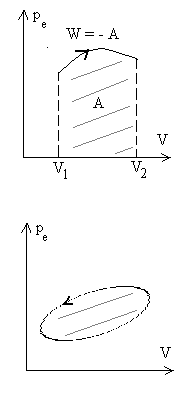 |
 = - aire entre la courbe, les droites
= - aire entre la courbe, les droites 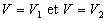 ,
laxe V. ,
laxe V.
Cas dun cycle : W > 0 si le cycle est décrit dans
le sens trigonométrique (ou positif)
W < 0 si le cycle est décrit dans le sens inverse (ou
négatif).
W > 0 le système est une machine réceptrice
W < 0 le système est une machine motrice |
Ces schémas montrent que le travail des forces de pression
extérieure dépend des états initial et final, des
états intermédiaires cest à dire de la transformation
amenant de létat initial à létat final (on dit du
chemin suivi).
3. Chaleur sensible. Chaleur latente
Lorsque léchange de chaleur a pour effet de faire varier la
température dun système sans changement de phase, on parle
de chaleur sensible. Par contre, sil sagit dun corps pur changeant
de phase à température constante, on parle de chaleur
latente (rappelons que, dans ce cas, la pression est constante -Chapitre
2-).
3.1. Chaleur sensible. Capacités calorifiques
Transformation à volume constant (transformation isochore)
Réalisation : il suffit que les parois qui délimitent
le système soient indéformables et fixes ; ceci est facilement
réalisable pour les systèmes gazeux, presque impossible pour
les liquides ou les solides (dont les volumes varient peu mais sur lesquels
il faudrait exercer des forces très importantes pour les empêcher
de changer de volume)
Pour un système fermé, le premier principe de la Thermodynamique
sécrit : 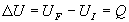 puisque le travail échangé est nul.
puisque le travail échangé est nul.
La fonction détat U dépend des variables détat 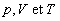 dont deux seulement sont indépendantes (existence dune équation
détat). Si nous imposons une condition (ici
dont deux seulement sont indépendantes (existence dune équation
détat). Si nous imposons une condition (ici  ),
il ny a plus quune variable indépendante. Nous choisissons la température
T comme variable indépendante ce qui veut dire que nous considérons
la pression p comme une fonction de la température.
),
il ny a plus quune variable indépendante. Nous choisissons la température
T comme variable indépendante ce qui veut dire que nous considérons
la pression p comme une fonction de la température.
Ainsi dans le cas dune transformation à volume constant 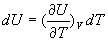 ,
la quantité
,
la quantité  est appelée capacité calorifique à volume constant,
l'unité de mesure dans le système MKSA est le J/K.
est appelée capacité calorifique à volume constant,
l'unité de mesure dans le système MKSA est le J/K.
Le caractère additif de U et intensif de T donne à  un caractère additif.
un caractère additif.
Pour un mélange, la capacité calorifique est la somme des
capacités de chacun des constituants ; pour un corps pur, le caractère
devient extensif cest à dire que 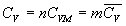 .
.
Le calcul de 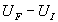 est indépendant de la transformation (en particulier de la nature réversible
ou non de la transformation), il ne dépend que des états initial
et final, soit
est indépendant de la transformation (en particulier de la nature réversible
ou non de la transformation), il ne dépend que des états initial
et final, soit

Sauf avis contraire, 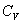 pourra être pris " constant " si bien que
pourra être pris " constant " si bien que  si la transformation est isochore (à volume constant).
si la transformation est isochore (à volume constant).
Transformation à pression constante (transformation isobare)
Réalisation : Le milieu extérieur impose une pression 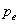 ; dans les états initial ou final, il y a équilibre entre des
pressions entre le milieu extérieur et le système ; lors de la
transformation, le volume du système varie, sa pression reste constante
(transformations quasistatique et réversible) ou devient non-uniforme
(transformation irréversible).
; dans les états initial ou final, il y a équilibre entre des
pressions entre le milieu extérieur et le système ; lors de la
transformation, le volume du système varie, sa pression reste constante
(transformations quasistatique et réversible) ou devient non-uniforme
(transformation irréversible).
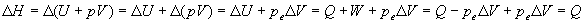
La fonction détat H dépend des variables détat 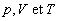 dont deux seulement sont indépendantes (existence dune équation
détat). Si nous imposons une condition (ici
dont deux seulement sont indépendantes (existence dune équation
détat). Si nous imposons une condition (ici  ),
il ny a plus quune variable indépendante. Nous choisissons la température
T comme variable indépendante ce qui veut dire que nous considérons
le volume V comme une fonction de la température.
),
il ny a plus quune variable indépendante. Nous choisissons la température
T comme variable indépendante ce qui veut dire que nous considérons
le volume V comme une fonction de la température.
Ainsi dans le cas dune transformation à pression constante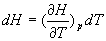 ,
la quantité
,
la quantité 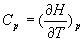 est appelée capacité calorifique à pression constante,
l'unité de mesure dans le système MKSA est le J/K.
est appelée capacité calorifique à pression constante,
l'unité de mesure dans le système MKSA est le J/K.
Le caractère additif de H et intensif de T donne à 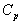 un caractère additif.
un caractère additif.
Pour un mélange, la capacité calorifique est la somme des
capacités de chacun des constituants ; pour un corps pur, le caractère
devient extensif cest à dire que 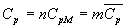 .
.
Le calcul de 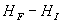 est indépendant de la transformation (en particulier de la nature réversible
ou non de la transformation), il ne dépend que des états initial
et final, soit
est indépendant de la transformation (en particulier de la nature réversible
ou non de la transformation), il ne dépend que des états initial
et final, soit
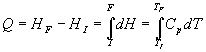
Sauf avis contraire, 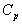 pourra être pris " constant " si bien que
pourra être pris " constant " si bien que 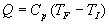 si la transformation est isobare (à pression constante).
si la transformation est isobare (à pression constante).
3.2. Chaleur latente de changement de phase (détat)
dun corps pur
Cette transition de phase qui seffectue à température
et pression constantes saccompagne de transferts dénergie.
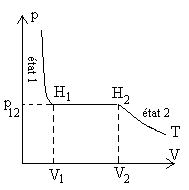 |
On appelle chaleur latente (massique ou molaire)
de changement détat dun corps pur à la température
T
la variation denthalpie (de lunité de masse ou dune mole) de
ce corps passant dun état (solide, liquide ou gazeux) à
un autre état. |
La notation habituelle pour les chaleurs latentes est L. Ainsi 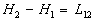 , la variation denthalpie pour aller de létat 1 à létat
2 est égale à la quantité de chaleur échangée
sur lisobare.
, la variation denthalpie pour aller de létat 1 à létat
2 est égale à la quantité de chaleur échangée
sur lisobare.
Les chaleurs latentes de fusion (transition solide à
liquide), de vaporisation (transition liquide à
vapeur) et de sublimation (transition solide à
gaz) sont positives cest à dire quil faut fournir de la chaleur
pour faire fondre un solide, vaporiser un liquide ou sublimer un solide.
Les chaleurs latentes de solidification, de condensation à létat
liquide et de condensation à létat solide sont respectivement
opposées à celles de fusion, de vaporisation et de sublimation.
3.3. Remarques
La Calorimétrie a pour objet la mesure des capacités calorifiques
et des chaleurs latentes. Le chapitre 7 " Propriétés de la
matière " apportera un certain nombre de connaissances essentielles
avant dentreprendre la façon de faire ces mesures.
A ce stade du cours, nous nous contenterons de dire que  et
et  se déduisent
lun de lautre et que cest la mesure de la capacité calorifique à
pression constante qui est le plus facilement accessible.
se déduisent
lun de lautre et que cest la mesure de la capacité calorifique à
pression constante qui est le plus facilement accessible.
En fait, pour les solides et les liquides,  et
et  sont
peu différents (quelques %), alors que, pour un gaz, les valeurs respectives
sont sensiblement différentes.
sont
peu différents (quelques %), alors que, pour un gaz, les valeurs respectives
sont sensiblement différentes.
Pour tous les corps,  est supérieur à
est supérieur à  (on introduit, de manière utile, le rapport
(on introduit, de manière utile, le rapport  ).
).
Les chaleurs latentes sont, dautre part, très importantes.
Nous ne donnons quun seul exemple : pour élever 1 kg deau
liquide de 0 °C à 100 °C, il faut 418
kJ
; pour transformer 1 kg deau liquide à 100 °C
en 1 kg de vapeur à la même température, il
faut 2253 kJ soit environ 4 fois plus.
On trouvera , à la fin du cours, dans lannexe " Détermination
expérimentale des caractéristiques thermodynamiques "
un certain nombre de résultats expérimentaux.
4. Etude énergétique
du gaz parfait
4.1. Fonctions détat U,
H
et S
4.1.1. Première loi de Joule
| Expérience de Joule Gay-Lussac
Une mole de gaz est enfermée dans un récipient R1.
On ouvre le robinet et le gaz se répartit dans les récipients
R1 et R2
.
Les parois des récipients sont indéformables et parfaitement
calorifugées de lextérieur si bien que la détente
du gaz seffectue à énergie interne constante.
Si la pression initiale dans R1 nest
pas trop élevée (gaz se comportant comme un gaz parfait),
la
température ne varie pas au cours de la détente. |
 |
Pour un gaz parfait, la température est constante si lénergie
interne est constante, soit  ou
ou 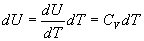 où
où  ne peut dépendre que de la température.
ne peut dépendre que de la température.
Ces résultats constituent la première loi de Joule et
sont conformes avec ce que nous avons exposé dans le Chapitre 2
4.1.2. Deuxième loi de Joule
| Expérience de Joule-Thomson |
|
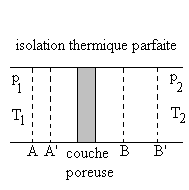
Un gaz à pression 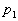 sécoule lentement en parcourant un tube horizontal à parois
parfaitement calorifugées. Il traverse une couche poreuse et sort
à la pression
sécoule lentement en parcourant un tube horizontal à parois
parfaitement calorifugées. Il traverse une couche poreuse et sort
à la pression 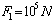 .
Un ventilateur permet de maintenir un régime permanent (débit
constant) dans lequel les pressions .
Un ventilateur permet de maintenir un régime permanent (débit
constant) dans lequel les pressions 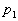 et
et 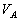 et
les températures en amont et en aval de la couche poreuse ne dépendent
pas du temps. et
les températures en amont et en aval de la couche poreuse ne dépendent
pas du temps.
On considère le système thermodynamique compris, à
linstant 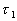 ,
entre les sections A et B. Compte tenu de lécoulement, ce système
à un instant ,
entre les sections A et B. Compte tenu de lécoulement, ce système
à un instant  se situe entre les sections A et B.
se situe entre les sections A et B. |
 |
Le travail échangé entre les instants 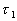 et
et 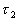 par le
système est égal à
par le
système est égal à 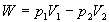 si
si  est la
partie de volume du système comprise entre les section A et A et
est la
partie de volume du système comprise entre les section A et A et 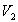 est la partie de volume du système comprise entre les section B et B.
est la partie de volume du système comprise entre les section B et B.
Le lecteur qui aurait quelques difficultés pourra imaginer
deux parois fictives situées initialement aux sections A et B ;
en fait, la vraie difficulté est quil sagit dun système
ouvert et que ceux-ci seront étudiés dans le chapitre 6.
Lécriture du principe de conservation (où on néglige
toute variation dénergie cinétique, écoulement à
faible vitesse, et toute variation dénergie potentielle, tube horizontal)
conduit à : 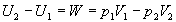 (
(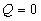 puisque les
parois sont parfaitement calorifugées).
puisque les
parois sont parfaitement calorifugées).
En réorganisant, on obtient : 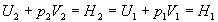 .
Lécoulement (la détente) de Joule-Thomson est un écoulement
(une détente) isenthalpique (à enthalpie constante)
.
Lécoulement (la détente) de Joule-Thomson est un écoulement
(une détente) isenthalpique (à enthalpie constante)
Si la pression 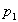 nest pas trop élevée (gaz se comportant comme un gaz parfait),
la température ne varie pas lors de la traversée de la couche
poreuse (
nest pas trop élevée (gaz se comportant comme un gaz parfait),
la température ne varie pas lors de la traversée de la couche
poreuse (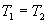 ).
).
Pour un gaz parfait, la température est constante si lenthalpie est
constante, soit 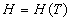 ou
ou  où
où 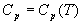 ne peut dépendre que de la température.
ne peut dépendre que de la température.
Ce résultat constitue la deuxième loi de Joule.
Remarques :
-
Ce résultat est conforme à nos connaissances actuelles.
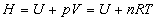 pour un gaz
parfait ð si lénergie interne ne dépend
que de la température, lenthalpie aussi.
pour un gaz
parfait ð si lénergie interne ne dépend
que de la température, lenthalpie aussi.
Avec les connaissances exposées dans le chapitre 7, on peut
montrer quun gaz qui obéit aux deux lois de Joule est un gaz parfait.
-
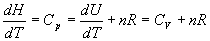
Ce résultat constitue la relation de Mayer : 
4.1.3. Fonctions détat du gaz parfait
- Lénergie interne dun gaz parfait se calcule à partir
de
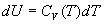 ð
ð 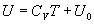 dans un intervalle de température où
dans un intervalle de température où 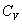 peut être pris constant (on trouve dans le chapitre 2 et dans lannexe
" Détermination expérimentale des caractéristiques thermodynamiques
" , des résultats et des explications quant aux valeurs de
peut être pris constant (on trouve dans le chapitre 2 et dans lannexe
" Détermination expérimentale des caractéristiques thermodynamiques
" , des résultats et des explications quant aux valeurs de 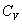 )
)
- Lenthalpie dun gaz parfait se calcule à partir de
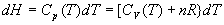 ð
ð 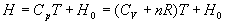 dans un intervalle de température où les capacités calorifiques
peuvent être prises constantes
dans un intervalle de température où les capacités calorifiques
peuvent être prises constantes
- Lentropie se calcule à partir de
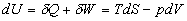 ð
ð 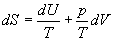
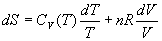 ð
ð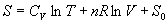 dans un intervalle de température où
dans un intervalle de température où 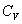 peut être pris constant.
peut être pris constant.
En utilisant 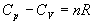 ,
, 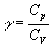 et
et 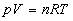 on obtient trois expressions équivalentes pour cette dernière
expression, à savoir
on obtient trois expressions équivalentes pour cette dernière
expression, à savoir
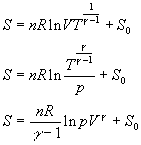
4.2. Etude
de quelques transformations pour un système fermé contenant un gaz
parfait
Pour toutes les transformations, les capacités calorifiques seront prises
constantes
4.2.1. Transformation isochore (V = Cste)
Pour une transformation réversible où
la température du système évolue progressivement de 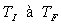 ,
,
on obtient : 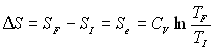 et
et 

Pour une transformation irréversible où
la source impose " brutalement " une température 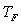 ,
,
on obtient : 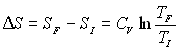 ,
, 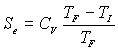 ;
; 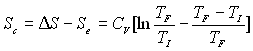
Le lecteur montrera que 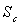 est positif quelques soient
est positif quelques soient  ; il pourra poser
; il pourra poser 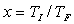 .
.
4.2.2. Transformation isobare (pression extérieure
pe )
Pour une transformation réversible où
la température du système évolue progressivement de 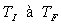 ,
,
on obtient :  et
et 

Pour une transformation irréversible où
la source impose " brutalement " une température 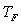 ,
,
on obtient :  ,
, 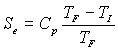 ;
; 
Le lecteur montrera que 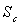 est positif quelques soient
est positif quelques soient  ; il pourra poser
; il pourra poser 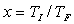 .
.
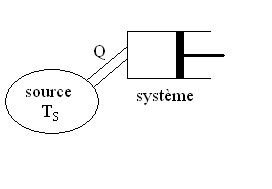
4.2.3. Transformation isotherme
|
Réalisation : Le système est
en contact avec une source de chaleur à température constante
TS ; dans les états initial ou final, il
y a équilibre des températures entre le milieu extérieur
et le système ; lors de la transformation, la température
du système reste constante (transformations quasistatique et réversible)
ou devient non-uniforme (transformation irréversible).
|
|
 (puisque
(puisque 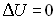 première
loi de Joule)
première
loi de Joule)
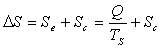
Pour une transformation réversible, 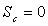 et
et 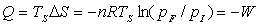
Autre démonstration : dW
= -pdV = Vdp = -dQ
Les variables p et V ne sont pas indépendantes puisque
liées par léquation détat pV=nRTS
On obtient : 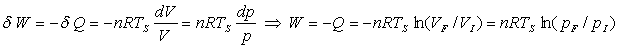
Pour une transformation irréversible où
la pression extérieure  est
imposée " brutalement ",
est
imposée " brutalement ",

Le calcul de lentropie créée par lirréversibilité
se fait à partir de : 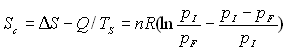 .
.
Le lecteur montrera que 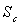 est positif quelques soient
est positif quelques soient  ; il pourra poser
; il pourra poser 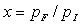 .
.
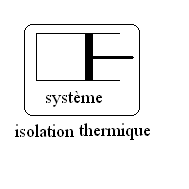
4.2.4. Transformation adiabatique (Q = 0)
|
Réalisation : Le système est
isolé thermiquement de lextérieur cest à dire que
les parois qui délimitent le système sont imperméables
à la chaleur (athermales) ; ceci peut être réalisé
par des parois constitués de matériaux non conducteurs de
la chaleur ou en éliminant le phénomène de convection
et en disposant des écrans anti-rayonnants pour éliminer
les échanges par radiations thermiques.
|
|
Le premier principe sécrit DU
= W, le second DS = Sc
.
Pour une transformation réversible, Sc
est nul donc aussi DS (ð
S est constant).
Une transformation adiabatique réversible est une transformation
isentropique.
En exploitant les formules de lentropie, on obtient une relation suivant
le couple de variables utilisées.
Si g est constant, on retient la relation
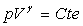 vraie à
chaque instant de la transformation, étant entendu quil est facile de
passer aux autres couples de variables en utilisant léquation détat
des gaz parfaits. Ce résultat est souvent appelé loi de Laplace.
vraie à
chaque instant de la transformation, étant entendu quil est facile de
passer aux autres couples de variables en utilisant léquation détat
des gaz parfaits. Ce résultat est souvent appelé loi de Laplace.
Ainsi, par exemple si le système initialement à pression  et température
et température 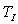 évolue jusqu'à un état final où la pression est
évolue jusqu'à un état final où la pression est
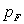 , la température
finale est
, la température
finale est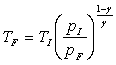 .
.
Le calcul le plus simple de W se fait à partir de 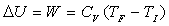 .
On peut aussi faire un calcul direct à partir de
.
On peut aussi faire un calcul direct à partir de 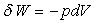 .
.
Pour une transformation irréversible, où,
sur le système initialement à pression  et température
et température 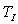 ,
on impose " brutalement " une pression extérieure constante
,
on impose " brutalement " une pression extérieure constante
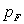 , on calcule W
par deux méthodes,
, on calcule W
par deux méthodes,
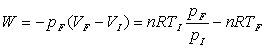 (application
directe de la formule de base)
(application
directe de la formule de base)
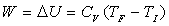
Nous disposons de deux relations indépendantes, de léquation
détat des gaz parfaits dans les états initial et final :
le problème thermodynamique est alors entièrement défini.
En les égalant et en organisant, on obtient 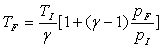
5. Transferts thermiques (transferts de chaleur
ou dénergie calorifique)
On appelle échangeur de chaleur le milieu solide qui sépare
le système de la source de chaleur. Une paroi de faible épaisseur,
de grandes dimensions transversales, est la représentation la plus
simple dun échangeur de chaleur.
5.1. Conduction de la chaleur
La non-uniformité de la température dans un solide entraîne
un transfert dénergie dun point à un autre. Ce transfert
qui se produit sans transport macroscopique de matière est
appelé " Conduction de la Chaleur ".
Il est régi par le loi de Fourier.
Dans les systèmes solides, seul ce mode de transfert est possible. Dans
les fluides, il peut être secondaire par rapport au transfert par convection.
Nous nous limitons à des solides homogènes et isotropes où,
en chaque point, existe un champ de température 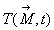
Loi de Fourier
Expérimentalement, si la variation spatiale de température
nest pas trop forte, le vecteur densité de flux de chaleur est égal
à : 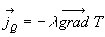
La densité de flux de chaleur j (flux de chaleur
par unité de surface transversale 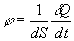 )
dans une direction caractérisée par un vecteur unitaire
)
dans une direction caractérisée par un vecteur unitaire 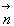 est :
est :
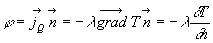
Ce type déquation est appelé équation de diffusion,
lécoulement de chaleur, qui se produit dans le sens des températures
les plus faibles, tend à uniformiser les températures.
Dans le système MKSA, j se
mesure en W.m-2 et
l
en W.m-1.K-1
.
l est appelé conductivité
thermique et traduit laptitude dun matériau à conduire
la chaleur.
Remarque : Lorsque, dans un milieu fluide, existent des gradients
de concentration de matière, il se produit des mouvements de matière
qui tendent à uniformiser la concentration de matière. Ce
phénomène de diffusion de matière est régi
par une loi analogue à celle de Fourier appelée loi de
Fick.
Quelques conductivités thermiques aux températures
ordinaires
| Ordre de grandeur de l
à 20 °C |
W m-1 K-1
|
| Gaz à la pression atmosphèrique |
0,006 - 0,18
|
| Matériaux isolants |
0,025 - 0,25
|
| Liquides non Métalliques |
0,1 - 1,0
|
| Solides non métalliques |
0,025 3
|
| Liquides métalliques |
8,5 85
|
| Alliages métalliques |
10 150
|
| Métaux purs |
20 400
|
| Ag |
418
|
Béton brut |
1,75
|
H2 |
0,18
|
| Cu |
390
|
Verre |
~ 1
|
He |
0,15
|
| Al |
238
|
Plâtre |
0,46
|
Ne |
0,05
|
| Laiton |
120
|
Bois |
0,25 à 0,12
|
O2 |
0,027
|
| Fe |
82
|
Laine de verre |
0,04
|
N2 |
0,026
|
| Pt |
69
|
Polystyrène |
0,04
|
Ar |
0,018
|
| Pb |
35
|
Eau |
0,6
|
CO2 |
0,017
|
| Ti |
20
|
Alcool |
0,17
|
Kr |
0,01
|
| Inox |
14
|
Huile minérale |
0,13
|
|
|
5.2. Echanges de chaleur à la frontière
dun solide
Convection de la chaleur
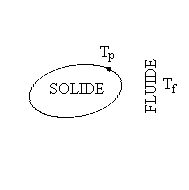 |
Cest le mode de transfert que lon observe
entre un solide et un fluide. Il comprend des phénomènes
de conduction auxquels se superpose un transport de matière, les
molécules du fluide venant se réchauffer ou se refroidir
au contact du solide.
Le transport de matière dans un fluide peut se faire de deux
manières :
-
naturelle les molécules chaudes de masse volumique plus faible
ont tendance à sélever.
|
-
forcée une pompe (ou un ventilateur) provoque le déplacement
du fluide dans une direction.
Létude de ces phénomènes, régis par les équations
de Navier-Stokes, ne peut être abordée sans de sérieuses
connaissances de Mécanique des fluides.
Nous resterons très élémentaire et poserons que
la densité de flux de chaleur échangée par convection
est égale à :
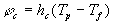 où hc
est le coefficient de convection, Tp la
température à la paroi du solide et Tf
la " température du fluide " au loin si celui-ci est " seul " ou la " température
de mélange " sil est entre deux parois.
où hc
est le coefficient de convection, Tp la
température à la paroi du solide et Tf
la " température du fluide " au loin si celui-ci est " seul " ou la " température
de mélange " sil est entre deux parois.
hc est de lordre de quelques
unités pour la convection naturelle des gaz, quelques dizaines pour
la convection forcée des gaz, quelques centaines pour la convection
naturelle des liquides et de quelques milliers pour la convection forcée
des liquides.
hc est exprimée en W.m-2.K-1.
Rayonnement thermique
La surface dun solide émet un rayonnement électromagnétique
complexe dénergie dautant plus grande que cette surface est à
température plus élevée.
Ce rayonnement se propage dans les milieux transparents. Lorsquil
rencontre un corps, il est totalement absorbé (corps noir), partiellement
absorbé (corps réfléchissants, semi-transparents)
ou pas du tout absorbé (corps parfaitement réfléchissants,
corps transparents). Lénergie absorbée est transformée
en énergie interne.
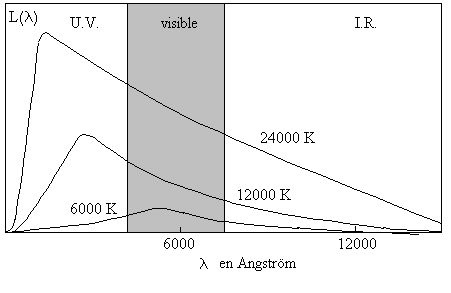
Le spectre du rayonnement électromagnétique dépend
de la température de surface du corps qui émet, de la nature
du corps et de son état de surface.
Laptitude dun corps à réfléchir, transmettre
ou absorber un rayonnement dépend aussi de ces paramètres.
Un bilan énergétique montre que, pour un corps en équilibre
thermique, son aptitude à absorber un rayonnement est identique à
son aptitude à en émettre. On rend compte de cette aptitude par
un coefficient  compris entre 0 et 1, appelé émissivité.
compris entre 0 et 1, appelé émissivité.
La densité de flux dénergie émise par un corps,
à température T, sous forme de rayonnement électromagnétique
est égale à 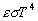 où
où 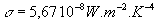 est la constante de Stéfan-Boltzmann.
est la constante de Stéfan-Boltzmann.
- pour des corps ternes (dit gris ; cas des peintures non métalliques,
des matériaux servant dans la construction), on peut considérer
que
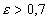 .
.
- pour des corps métalliques polis (brillants et donc réfléchissants),
 se situe dans la fourchette de valeurs 0,05 - 0,3
se situe dans la fourchette de valeurs 0,05 - 0,3
Les échanges dénergie par rayonnement entre deux corps
dépendent de leur position relative.
En restant très élémentaire, la densité de flux de
chaleur échangée par rayonnement est : 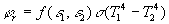
 est une fonction
des émissivités des surfaces et de leur position relative.
est une fonction
des émissivités des surfaces et de leur position relative.
-
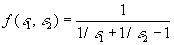 dans le cas
de deux surfaces planes, parallèles, de grandes dimensions
dans le cas
de deux surfaces planes, parallèles, de grandes dimensions
-
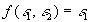 si la surface
démissivité
si la surface
démissivité 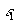 est convexe et entièrement entourée par une surface de très
grande dimension.
est convexe et entièrement entourée par une surface de très
grande dimension.
En remarquant que 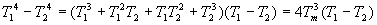 si Tm est une température moyenne
entre T1 et T2.
si Tm est une température moyenne
entre T1 et T2.
La densité de flux de chaleur échangée par rayonnement peut
être linéarisée sous la forme  avec
avec 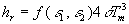 .
.
Cette linéarisation est très utilisée lorsque
les températures T1 et T2
sont voisines car hr , coefficient
de rayonnement, est pratiquement constant.
Pour en savoir plus
Dans une direction 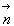 ,
la puissance énergétique spectrale (flux énergétique)
,
la puissance énergétique spectrale (flux énergétique) 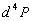 dun rayonnement de longueur donde compris entre
dun rayonnement de longueur donde compris entre 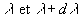 ,
émis (ou absorbé) par un élément de surface
,
émis (ou absorbé) par un élément de surface 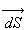 dans
un angle solide
dans
un angle solide  est donnée par la relation :
est donnée par la relation :
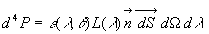 où
où 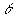 est langle entre
est langle entre 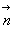 et
et 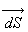 et
et 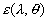 lémissivité spectrale dans la direction considérée.
lémissivité spectrale dans la direction considérée.
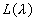 est la luminance
spectrale du corps noir qui est un corps qui absorbe tout rayonnement
[
est la luminance
spectrale du corps noir qui est un corps qui absorbe tout rayonnement
[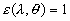 ].
].
Suivant une théorie de Planck introduisant la notion
de quantum dénergie,
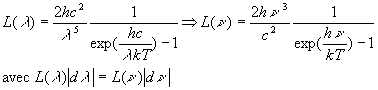
La valeur  correspondant
à un maximum de la luminance spectrale est donnée par la loi de
Wien, à savoir
correspondant
à un maximum de la luminance spectrale est donnée par la loi de
Wien, à savoir  .
.
Pour les corps obéissant à la loi de Lambert (les métaux
nobéissent pas à cette loi), lémissivité ne dépend
pas de la direction [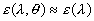 ],
],
ð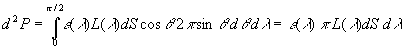
La quantité  est
appelé émittance spectrale
est
appelé émittance spectrale
On en déduit, si lémissivité ne dépend
pas de la longueur donde, la densité de flux énergétique
émise par rayonnement :
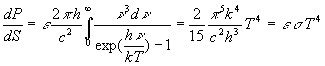
6. Bilans énergétiques
simples faisant intervenir les transferts thermiques
6.1. Paroi solide inerte déchangeur en régime
permanent
Pour ce type de système, il ny a pas, au cours du temps, de
variation de son énergie totale, ni déchange de travail
avec le milieu extérieur puisque le volume est constant.
Le principe de conservation de lénergie impose quà
chaque instant la chaleur échangée est nulle.
Mathématiquement, on écrit que le flux de chaleur 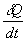 échangé par le système est nul (à chaque instant,
le flux de chaleur
échangé par le système est nul (à chaque instant,
le flux de chaleur 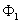 " entrant " est égal au flux de chaleur
" entrant " est égal au flux de chaleur 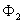 " sortant ", soit
" sortant ", soit 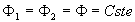 puisque le régime est permanent).
puisque le régime est permanent).
Dans le cas particulier où, dans le bilan énergétique,
seuls interviennent des échanges de chaleur, on emploie lexpression
bilan
thermique.
6.1.1. Paroi en forme de " mur "
En thermique, on appelle " mur " un système où les échanges
de chaleur se produisent suivant une direction cartésienne, par
exemple x.
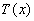 représente
donc le champ de température en régime permanent.
représente
donc le champ de température en régime permanent.
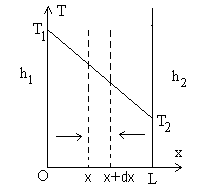 |
Le bilan thermique est fait sur un élément
de volume adapté, dans ce cas celui compris entre les abscisses
x
et x+dx de surface transversale S arbitraire.
Suivant la loi de Fourier, le flux de chaleur " entrant " par conduction
par la face x est égal à 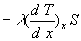 ,
celui " sortant " par la face x+dx est égal à ,
celui " sortant " par la face x+dx est égal à 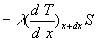 .
. |
Le bilan thermique consiste à écrire que le flux de chaleur
qui entre est égal à celui qui sort.
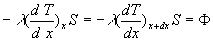 ð
ð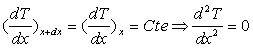
La résolution, avec les deux conditions aux limites 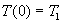 et
et 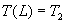 , conduit
à
, conduit
à  et
et 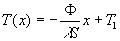
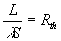 représente
la résistance thermique pour une section transversale S
et
représente
la résistance thermique pour une section transversale S
et 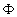 le flux
de chaleur. Nous pouvons faire une analogie avec le domaine électrique
en régime permanent entre différences de température et
différence de potentiel dune part et, dautre part, flux de chaleur
et intensité du courant électrique.
le flux
de chaleur. Nous pouvons faire une analogie avec le domaine électrique
en régime permanent entre différences de température et
différence de potentiel dune part et, dautre part, flux de chaleur
et intensité du courant électrique.
- A la frontière du solide, en
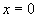 et
et 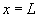 , les
échanges de chaleur se produisent respectivement avec des fluides à
température
, les
échanges de chaleur se produisent respectivement avec des fluides à
température 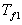 et
et 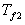 par
lintermédiaire de coefficients déchanges de chaleur
par
lintermédiaire de coefficients déchanges de chaleur 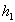 et
et 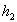 .
.
Le bilan énergétique (thermique) permet décrire :
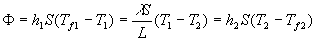
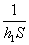 et
et  apparaissent comme les résistances thermiques liées au coefficients
apparaissent comme les résistances thermiques liées au coefficients 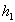 et
et 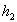 et
et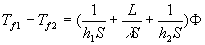
Remarque : utilisation d " ailettes ou barres " pour augmenter les
échanges de chaleur
On place, aux frontières de la paroi, des solides de forme particulière
appelés " ailettes ou barres ". Laugmentation des échanges
de chaleur (diminution de la résistance thermique) est obtenue par
laugmentation de la surface déchange avec les fluides extérieurs.
Ces solides sont de forme allongée, cest à dire possèdent
des dimensions transversales faibles par rapport à la troisième
dimension.
Le gradient de température a lieu principalement dans le sens
de cette dernière direction. Chaque section transversale est, en
première approximation, à température uniforme ce
qui nest pas contradictoire avec le fait de considérer des échanges
de chaleur suivant ces directions jusquau contact avec le fluide extérieur.
L efficacité 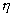 dune ailette est définie par le rapport du flux de chaleur échangé
par lailette au flux de chaleur qui serait échangé si elle nexistait
pas.
dune ailette est définie par le rapport du flux de chaleur échangé
par lailette au flux de chaleur qui serait échangé si elle nexistait
pas.
Des notions complémentaires sur les ailettes seront abordées
en travaux dirigés.
Pour en savoir plus
-
Examinons le cas de deux murs " accolés " (de même section
avec une face commune)
 |
Un bilan thermique entre deux sections quelconques
prises dans chacun des deux murs conduit à :
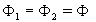
Par suite,
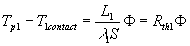 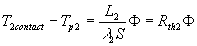 |
Le problème posé est celui de lécart 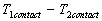 .
.
Lextrapolation jusquau contact du champ de température dans le milieu
1 conduit à la valeur  qui est, à priori, différente de
qui est, à priori, différente de 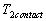 température
dextrapolation jusquau contact dans le milieu 2.
température
dextrapolation jusquau contact dans le milieu 2.
Pour tenir compte de cet écart, on introduit une résistance
thermique supplémentaire appelée résistance thermique
de contact suivant la relation 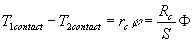
Les valeurs de la résistance de contact sont sensibles
si la conductivité du fluide interstitiel est très différente
de celles constituant les matériaux en contact, donc dans le cas
de matériaux en contact conducteurs.
Si lécart 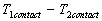 est négligeable, on dit que le contact est parfait.
est négligeable, on dit que le contact est parfait.
On remarque, de plus, que 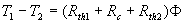
6.1.2. Paroi à symétrie de révolution. Paroi
à symétrie sphérique
Symétrie de révolution autour dun axe
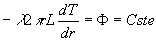 ;
; 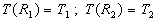 où r est la distance à laxe et L une longueur axiale arbitraire.
où r est la distance à laxe et L une longueur axiale arbitraire.
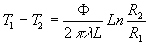 et
et 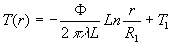 .
.
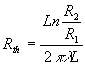 représente
la résistance thermique (
représente
la résistance thermique (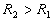 ).
).
Symétrie sphérique
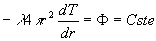 ;
; 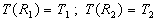 où r est la distance au centre de symétrie.
où r est la distance au centre de symétrie.
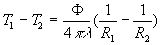 et
et
 représente
la résistance thermique (
représente
la résistance thermique (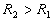 ).
).
6.2. Bilans énergétiques pour un solide
en régime transitoire
Entre deux instants successifs t et t + dt, le premier
principe de la Thermodynamique pour un système peut être écrit
:
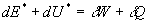 où
où
-
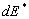 doit être
compris comme la transformation au sein du milieu dénergie potentielle,
dénergie chimique ou nucléaire en énergie calorifique
; il sagit de leffet Joule ou de lénergie calorifique résultat
dune réaction exothermique ou endothermique (nous appelons sources
de chaleur internes ce type dénergie)
doit être
compris comme la transformation au sein du milieu dénergie potentielle,
dénergie chimique ou nucléaire en énergie calorifique
; il sagit de leffet Joule ou de lénergie calorifique résultat
dune réaction exothermique ou endothermique (nous appelons sources
de chaleur internes ce type dénergie)
-
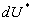 est la variation
dénergie interne résultant de variations des variables détat
est la variation
dénergie interne résultant de variations des variables détat
-
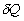 représente
les échanges de chaleur aux frontières du système
représente
les échanges de chaleur aux frontières du système
-
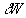 représente
les échanges de travail aux frontières du système.
représente
les échanges de travail aux frontières du système.
Le système solide subit une transformation à pression 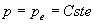
 variation denthalpie
résultant de variation dans le temps du champ de température.
variation denthalpie
résultant de variation dans le temps du champ de température.
6.2.1. Cas où la température du solide est uniforme
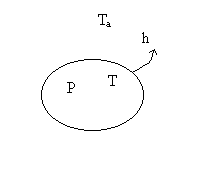 |
On considère un milieu de volume V,
de surface S, de capacité calorifique 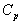 ,
siège dune dissipation dénergie de puissance ,
siège dune dissipation dénergie de puissance 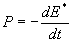 . .
La température extérieure 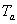 est constante, celle du milieu
est constante, celle du milieu  est uniforme . On appelle h le coefficient déchange traduisant
les échanges de chaleur par convection et/ou rayonnement.
est uniforme . On appelle h le coefficient déchange traduisant
les échanges de chaleur par convection et/ou rayonnement. |
Le bilan thermique conduit à 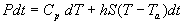 ,
soit
,
soit 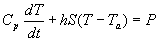
En régime permanent, on obtient 
Pour en savoir plus
6.2.2. Equation de la chaleur
On considère un élément
du milieu quelconque, suffisamment petit pour être homogène,
de volume V, limité par une surface S.
-
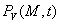 est la puissance calorifique volumique des sources internes, si bien
que
est la puissance calorifique volumique des sources internes, si bien
que 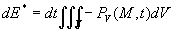
|
 |
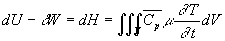 où
où 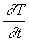 est lélévation de température par unité de temps,
est lélévation de température par unité de temps,  et
et 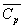 respectivement
la masse volumique et la capacité calorifique massique à pression
constante du milieu (on remarquera que, dans le cas dune évolution
à volume constant, il conviendrait de remplacer la capacité
calorifique à pression constante par celle à volume constant
et que la différence nest significative que dans le cas des gaz).
respectivement
la masse volumique et la capacité calorifique massique à pression
constante du milieu (on remarquera que, dans le cas dune évolution
à volume constant, il conviendrait de remplacer la capacité
calorifique à pression constante par celle à volume constant
et que la différence nest significative que dans le cas des gaz).
- Les échanges de chaleur aux frontières du milieu sexpriment,
compte tenu de lorientation de la normale
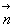 ,
par la relation
,
par la relation 
Lapplication du premier principe de la Thermodynamique conduit à léquation
de la chaleur,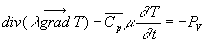
Pour des conductivités thermiques indépendantes de
la température et des milieux isotropes, on obtient :
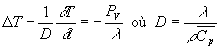 est la diffusivité
thermique (m2.s-1).
est la diffusivité
thermique (m2.s-1).
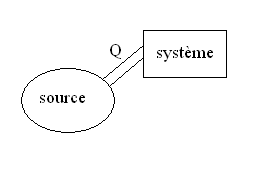
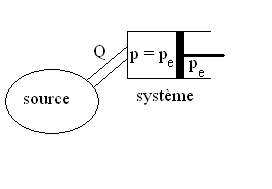
6.3. Bilan énergétique pour un fluide
en écoulement permanent
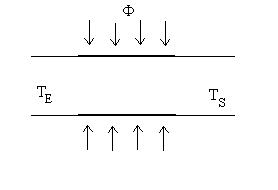 |
Lécoulement permanent dun fluide seffectue
à pression constante.
Il reçoit un flux de chaleur 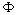 si bien que sa température évolue dune valeur amont (à
lentrée)
si bien que sa température évolue dune valeur amont (à
lentrée) 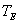 à une valeur aval (à la sortie)
à une valeur aval (à la sortie) 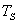 . .
Une quantité de masse dm de fluide échange la quantité
de chaleur  si
on néglige, pour le fluide, toute variation dénergie cinétique
et potentielle. si
on néglige, pour le fluide, toute variation dénergie cinétique
et potentielle. |
Par unité de temps, on écrit 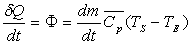 où
où 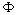 est le flux de chaleur échangé par le fluide.
est le flux de chaleur échangé par le fluide.


 = - aire entre la courbe, les droites
= - aire entre la courbe, les droites 
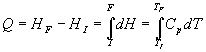



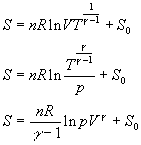
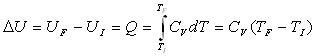
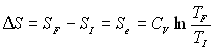 et
et 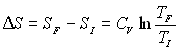 ,
, 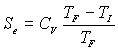 ;
; 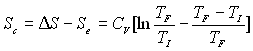
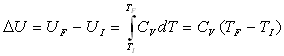
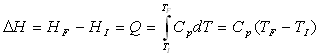
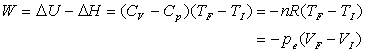
 et
et  ,
, 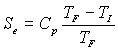 ;
; 


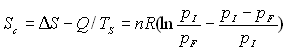 .
.
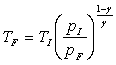 .
.
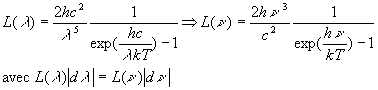

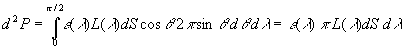
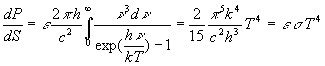
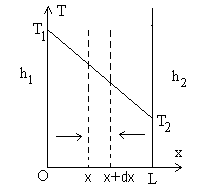

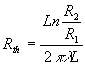 représente
la résistance thermique (
représente
la résistance thermique ( représente
la résistance thermique (
représente
la résistance thermique (

