CHAPITRE 3 : Les Premier et Second Principes
Plan
Le Premier Principe
1. Notion de conservation de lénergie
2. Premier Principe de la Thermodynamique
2.1. Modification de létat dun système
2.2. Principe déquivalence
2.3. Energie interne
2.4. Premier Principe de la Thermodynamique pour
un système fermé
3. Mécanique et Thermodynamique. Principe de
conservation de lénergie
Le Second Principe
1. Le Second Principe pour un système fermé
1.1. Enoncé
1.2. Entropie dun système isolé fermé
1.3. Remarques
1.4. Conséquences mathématiques des
premier et second principes
2. Les énoncés historiques de Clausius
et Thomson
2.1. Enoncé de Clausius
2.2. Enoncé de Thomson
3. Les causes dirréversibilité
Annexe : quelques rappels simples de Mécanique
Le Premier Principe
Tout domaine des Sciences Physiques introduit le concept dénergie.
Bien que ce concept soit récent (environ deux siècles), il
a largement dépassé le champ de compétences des Sciences
Physiques et il nest pas exagéré de dire quil conditionne
" lordonnancement de nos vies sur la planète Terre " : le moindre
" dérèglement " dans lapprovisionnement énergétique
est source de conflits et dinterventions rapides.
1. Notion de conservation de lénergie
Le lecteur pourra utiliser avec avantage, si nécessaire, lannexe
"
Quelques rappels simples de Mécanique " située à
la fin du chapitre.
Le mot énergie vient du grec energhia
qui signifie " force en action " cest à dire capacité à
produire un mouvement.
Ainsi un corps qui possède de lénergie cinétique
(jadis appelée " force vive ") peut continuer, de lui-même,
son mouvement au moins sur une certaine distance même dans un milieu
résistant (sopposant au mouvement).
Lénergie potentielle (jadis appelée " force morte ") a
la capacité à produire un mouvement puisque, spontanément,
par exemple, un corps pesant non contraint chute, une particule chargée
q non contrainte à potentiel électrique V (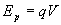 )
se met en mouvement vers des régions de moindre énergie électrique.
)
se met en mouvement vers des régions de moindre énergie électrique.
En Mécanique, on apprend :
- que forces et énergie cinétique apparaissent ensemble
dans le théorème de lénergie cinétique,
- que lénergie potentielle est liée à la notion
de forces conservatives cest à dire de forces qui conservent lénergie
mécanique.
Très vite, le concept dénergie mécanique se révèle
insuffisant.
Un opérateur exerce une action (force) sur un système
qui acquiert de lénergie mécanique. Dans un certain nombre
de cas il se trouve que le travail de lopérateur est égal
à lénergie mécanique acquise par le système.
Ceci est satisfaisant pour lesprit humain attaché à
la notion de conservation : lénergie acquise par le système
a été perdue par lopérateur qui a pu la transmettre
(léchanger) par travail.
Comment interpréter si le travail de lopérateur nest
pas égal à lénergie mécanique acquise par
le système ? Ceci se produit lorsquil y a " des frottements, des
résistances " et lénergie mécanique acquise est toujours
inférieure au travail de lopérateur.
L énergie de lUnivers diminue telle ? Y a til possibilité
dune création spontanée dénergie qui compenserait
partiellement, totalement la perte dénergie, voire la dépasserait
ce qui ferait que lénergie de lUnivers augmenterait.
La réponse à ces questions constitue le Principe de
conservation de lénergie.
2. Premier Principe de la Thermodynamique
2.1. Modification de létat dun système
par échange dénergie sous forme de travail de forces
dopérateur extérieur
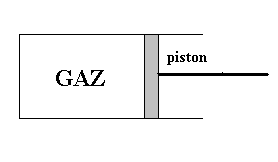 |
Un gaz est enfermé dans un récipient
(cylindre) dont lune (piston) des parois solides est mobile. Un opérateur
extérieur en exerçant une force sur le piston provoque le
déplacement de ce dernier et, par exemple, une diminution du volume
occupé par le gaz. Il se produira une augmentation de la pression
du gaz et, généralement, une variation de la température
du gaz. |
Létat du système gaz a changé.
Lopérateur a effectué un travail qui, suivant ce que
nous a appris la Mécanique, est un échange dénergie
entre le système gaz et lopérateur extérieur. Cet
échange dénergie se traduit par une modification des variables
détat.
par transferts thermiques (ou transfert de chaleur ou transfert dénergie
calorifique)
Lorsque nous mettons en " contact " des corps de températures
différentes, nous produisons une modification de létat
de ces corps (changement des températures et/ou de phases).
Leau contenue dans une casserole en contact avec la flamme dun gaz
en combustion voit sa température sélever puis elle se met
à bouillir cest à dire elle se transforme en vapeur (gaz).
Nous ne pouvons attribuer ces modifications de létat du système
à des échanges dénergie sous forme de travail.
Dans ce cas, nous parlons de transferts thermiques (ou de transfert
de chaleur).
Cependant, il ne faudrait pas croire que ces deux façons dagir
sur un système peuvent être totalement équivalentes
: par transferts thermiques, nous ne pouvons jamais affecter directement
le mouvement dun système.
2.2. Principe déquivalence
Nous sommes tout à fait capables délever la température
de leau contenue dans une casserole en mettant en mouvement des palettes
solides (agitateur). Nous produisons des effets tout à fait comparables
à ceux produits par transferts thermiques mais cette fois par échange
dénergie sous forme de travail.
Est-ce que les transferts thermiques (la chaleur) sont une autre façon
déchanger de lénergie entre différents systèmes
?
La question a été longtemps débattue au 19ème
siècle. La réponse fait partie du Principe déquivalence
à savoir que travail de forces et chaleur sont les deux seules
façons possibles déchanger de lénergie entre systèmes
fermés.
Les travaux de J. Joule au siècle dernier ont été
déterminants.
Dans un calorimètre (récipient contenant de leau dont
les parois peuvent être parfaitement isolées dun point de
vue thermique), Joule, dans un premier temps, élevait la température
par échange dénergie sous forme de travail (W était
fourni au calorimètre et compté positivement), dans un deuxième
temps, il ramenait le calorimètre à son état initial
en le refroidissant par échange de chaleur avec lextérieur
(la chaleur Q était perdue par le calorimètre et compté
négativement).
Les mesures de Joule, sur ce cas expérimental, montrèrent que 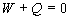
Ce résultat suppose que travail et chaleur soient comptés
dans une même unité.
En fait, avant Joule, les quantités de chaleur étaient
comptées en calories, la calorie étant la quantité
de chaleur nécessaire pour élever 1g deau de 14,5
à 15,5 °C sous la pression atmosphérique normale.
Les expériences de Joule établissent un rapport entre
lunité travail (appelé actuellement Joule) et lunité
chaleur compris entre 4,1855 et 4,1860.
1 cal = 4,18 joules
Le résultat 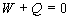 généralisé à tout système constitue le principe
déquivalence que nous énoncerons ainsi :
généralisé à tout système constitue le principe
déquivalence que nous énoncerons ainsi :
" Dans une expérience dans laquelle rien na varié dautre
que des quantités de travail et de chaleur échangées
avec lextérieur, il y a équivalence entre le travail et
la chaleur "
ou
" Lorsquun système thermodynamique fermé quelconque
subit un cycle de transformations qui le ramène à son état
initial, la somme du travail W et de la chaleur Q échangés
est nulle "
2.3. Energie interne
Définition de lénergie interne
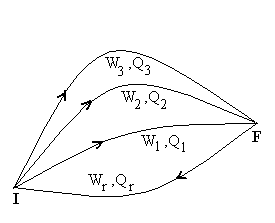
La quantité W + Q est indépendante de la transformation
amenant de létat I à létat F. Elle ne dépend donc
que des états I et F dont on rend compte par les variables détat.
Par définition, la somme W + Q est la variation
de lénergie interne U du système soit :
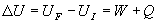
Définie par une variation, lénergie interne U
nest connue quà une constante additive près. Elle ne dépend
que de létat du système.
Pour un système en état déquilibre où
les variables détat (cest à dire les paramètres
mesurables qui rendent compte de létat du système) sont
constantes et uniformes, lénergie interne est une fonction de celles-ci
: par définition, on appelle fonction détat une fonction
des variables détat.
Aussi lénergie interne U est une fonction détat 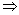 U
= U(variables détat)
U
= U(variables détat)
Visualisation de lénergie interne
Compte tenu de ce que nous savons sur la structure de la matière, de
lénergie cinétique qui ne fait appel quà laspect macroscopique
du système et de lénergie potentielle qui est le résultat
dinteractions avec dautres systèmes macroscopiques, lénergie
interne est une notion simple qui comprend :
- lénergie cinétique " microscopique " des particules constituant
le système dans un référentiel où les particules
sont globalement au repos,
- lénergie des interactions entre particules,
- lénergie de liaison des molécules (énergie chimique),
- lénergie de liaison des constituants de latome (énergie atomique
ou nucléaire).
Une propriété importante de lénergie interne découle
de ce propos : lénergie interne a un caractère additif.
2.4. Premier Principe de la Thermodynamique pour un système
fermé
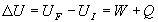
-
U énergie interne est une fonction détat ; sa variation
est indépendante de la transformation et ne dépend que des
états initial et final.
-
Lénergie interne a un caractère additif.
-
Le terme W représente le travail de forces produites par
un opérateur extérieur qui affectent létat thermodynamique
(variables détat) du système et Q représente
la chaleur. Ce sont les deux façons, pour un système fermé
isolé mécaniquement, déchanger de lénergie
avec dautres systèmes appelés milieu extérieur.
-
Puisquil sagit déchanges, il serait fondamentalement faux
dattribuer
travail et/ou chaleur à un système particulier.
-
W et Q dépendent de la transformation qui amène
dun état initial à un état final.
- En cohérence avec la Mécanique, ils sont comptés positivement
pour un système sils sont reçus par celui-ci, négativement
sils sont perdus (ou fournis) par le système.
Pour une transformation quasi-statique, entre deux états déquilibre
infiniment proches, le premier principe sécrit :
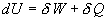
où dU est la variation élémentaire dune
fonction (mathématiquement, cest une différentielle totale
exacte),
où  sont
des quantités élémentaires qui ont laspect de formes différentielles
(ce ne sont pas des différentielles totales exactes, les fonctions
W et Q nexistent pas).
sont
des quantités élémentaires qui ont laspect de formes différentielles
(ce ne sont pas des différentielles totales exactes, les fonctions
W et Q nexistent pas).
On notera la différence de notation entre une différentielle
dune fonction (par exemple 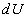 )
et une forme différentielle qui nest pas différentielle dune
fonction (par exemple
)
et une forme différentielle qui nest pas différentielle dune
fonction (par exemple  ).
).
Remarque : Très souvent pour les systèmes que nous
étudierons (nous ne disons pas pour le milieu extérieur)
les variations dénergie interne se limiteront à des changements
dénergie mécanique microscopique (pas de réactions
chimiques ou nucléaires).
3. Mécanique et Thermodynamique.
Principe de conservation de lénergie
Nous avions conclu le paragraphe 1 de ce chapitre sur un certain nombre de
questions pour lesquelles nous sommes, en mesure, de répondre avec l'introduction
du concept d'énergie interne et le principe de conservation de l'énergie.
Dans un référentiel, l'énergie totale d'un système est égale à 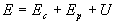
Mécanique et Thermodynamique mettent en évidence les notions d'énergies propres
à un système et les possibilités d'échanges d'énergie entre systèmes mais, à
ce stade de nos propos, il convient de noter une différence importante entre
les deux matière :
- en Thermodynamique, lorsqu'un système reçoit ou perd de l'énergie interne
un autre système a fourni ou a reçu cette énergie,
- En Mécanique, il y a possibilité de perte d'énergie mécanique s'il y a frottement.
Notre interrogation, à la fin du paragraphe 1 était : Qu'est devenue cette
énergie mécanique perdue ?
et la réponse constitue le Principe de conservation de l'énergie.
Pour un système dont l'énergie mécanique et l'énergie interne peuvent varier,
nous postulons la conservation de l'énergie, à savoir
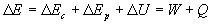
Si nous considérons le frottement entre mobiles,
- en Mécanique, on traduira le frottement par des forces qui affectent le mouvement
des mobiles et on déduira les pertes d'énergie mécanique,
- en Thermodynamique, on s'intéressera, à partir de la connaissance des pertes
d'énergie mécanique, aux augmentations d'énergie interne des mobiles et aux
échanges de chaleur avec un (éventuel) milieu extérieur.
Pour un effet Joule (perte d'énergie potentielle par frottement dans un système
électrique), la Thermodynamique cherchera à connaître les variations d'énergie
interne du système et ses échanges de chaleur avec un (éventuel) milieu extérieur.
Les échanges de chaleur ne sont possibles que s'il y a des différences de température
entre systèmes en contact thermique. Ces différences de température sont liées
à l'augmentation d'énergie interne, fonction d'état. Nous verrons qu'à pression
constante (ce qui est le cas d'un nombre important de transformations de notre
environnement quotidien) une augmentation d'énergie interne se traduit par une
augmentation de température.
Aussi, affirmer, comme il est écrit souvent ou comme nous l'entendons de la
part d'éminents collègues que "le travail des forces de frottement (perte
d'énergie mécanique) devient de la chaleur" nous paraît souvent révélateur
d'une méconnaissance de la notion d'énergie interne.
Cette phrase est vraie dans l'absolu c'est à dire au stade ultime des transformations
où les systèmes finissent toujours par se refroidir dans notre environnement
et augmenter la température moyenne de la planète Terre.
En résumé,
Toute augmentation (ou diminution) de l'énergie totale (globale) d'un système
s'accompagne d'une diminution égale (ou augmentation égale) de l'énergie totale
d'autres systèmes : La création spontanée d'énergie
n'existe pas.
Dans notre monde moderne, nous consommons énormément d'énergie interne dans
les réactions chimiques (combustion) ou nucléaires. Nous transformons cette
énergie dans les moteurs thermiques en énergie mécanique. Nous utilisons cette
énergie sous cette forme ou, après transformation, sous forme d'énergie électrique.
Une fois utilisée, nous avons une augmentation de l'énergie mécanique microscopique
de notre environnement ... inutilisable et la température moyenne de la planète
augmente.
Premier principe de la Thermodynamique pour un système
ouvert.
La matière contient de lénergie, il y a donc une autre
possibilité déchanger de lénergie : échanger
de la matière. Notre écriture du principe de conservation
de lénergie nest donc pas étendue au cas de léchange
de matière.
Dans le cadre de ce cours, nous aborderons le transfert dénergie
accompagnant léchange de matière dans le chapitre 6 " Notions
simples sur les systèmes ouverts ".
En conséquence, la quantité de matière est enfermée
et donc constante : elle ne peut être considérée comme
une variable de létat du système.
Nous aurons besoin dans la suite de ce cours de la fonction détat enthalpie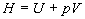 . Cette fonction nous paraîtra utile, facilitant les calculs. Son
sens physique sera donné lors du chapitre 6.
. Cette fonction nous paraîtra utile, facilitant les calculs. Son
sens physique sera donné lors du chapitre 6.
Le Second Principe
Le Second Principe (appelé en France Principe de S. Carnot) est
né, au début de lère industrielle entre 1810 et 1860
des réflexions menées sur le fonctionnement des machines
thermiques. En fait, outre S. Carnot, il convient de citer les travaux
de R. Clausius, G.A. Hirn et W. Thomson anobli en Lord Kelvin.
Lexpérience montre que certaines transformations qui satisferaient
le Premier Principe ne se produisent pas, par exemple,
- lénergie thermique se transfère spontanément
du corps chaud vers le corps froid,
- lors du freinage dune voiture la température des freins sélèvent
; de lénergie cinétique a été transférée
sous forme thermique au système de freinage; par contre, il nest
pas possible de mettre en marche une voiture en prenant de lénergie
thermique aux freins,
- un système subissant des évolutions cycliques ne peut
transformer de la chaleur en travail (moteur thermique) sil ne peut être
en contact avec au moins deux milieux extérieurs à températures
différentes,
- etc,
et quil est donc nécessaire dintroduire un Second Principe.
Les raisonnements qui ont permis une formulation générale
à partir de ces premières observations sont délicats
et, depuis le milieu du 19ème siècle, il a été
lobjet
de nombreuses recherches, en particulier son interprétation statistique
a largement contribué au développement didées apparues
au début du 20ème siècle.
Ainsi actuellement, le Second Principe dépasse largement un
cadre dapplications liées aux machines et nous adopterons une présentation
axiomatique inspirée par les travaux dI. Prigogine dans les années
1950.
Cette démarche pédagogique fait apparaître les
énoncés de Clausius ou Thomson, le fonctionnement des machines
thermiques comme des conséquences justificatrices de la validité
du Second Principe.
1. Le Second Principe pour un système
fermé
1.1. Enoncé
A tout système est associée une fonction détat
appelée entropie et notée S.
Lentropie est une grandeur additive.
Au cours dune transformation dun système fermé la variation
dentropie dun état initial à un état final est égale
à :
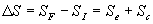
-
 est lentropie
échangée avec le milieu extérieur. Elle est comptée
positivement si elle est reçue par le système, négativement
dans le cas contraire.
est lentropie
échangée avec le milieu extérieur. Elle est comptée
positivement si elle est reçue par le système, négativement
dans le cas contraire.
-
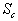 est lentropie
créée au sein du système.
est lentropie
créée au sein du système.
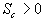 pour les transformations
irréversibles,
pour les transformations
irréversibles,  pour les transformations réversibles.
pour les transformations réversibles.
Cest cette inégalité qui traduit le fait que certaines
transformations ne sont pas possibles.
Contrairement à lénergie, lentropie ne se conserve
pas.
Entropie échangée
On appelle source de chaleur tout milieu extérieur envisagé
dans sa capacité à échanger de lénergie calorifique
(thermique) avec le système.
Remarque : le mot source ne doit surtout pas faire penser que le milieu
extérieur contient de la chaleur ; le milieu extérieur contient
de lénergie cinétique, potentielle, interne.
Nous limiterons nos propos à des sources de chaleur à
température uniforme.
Si d Q est la quantité de chaleur
échangée par le système entre les instants t et
t + dt avec une source à température TS
, lentropie d Se
échangée sera : 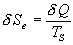
-
Cas dune source de chaleur à température constante
Le milieu extérieur échange de la chaleur sans changer
de température -milieu extérieur régulé en
température (thermostat) ou à très forte capacité
calorifique (eau dun lac, dune rivière, de mer, air atmosphérique,
...-.
Pendant lintervalle de temps Dt
où système et milieu extérieur sont en contact thermique,
ils échangent une quantité de chaleur Q et une entropie
Se
= Q / TS .
-
Cas de n sources de chaleur à température constante
Soit Qi la quantité de
chaleur échangée par le système avec la source i à
température Ti . Au cours
de la transformation, les sources sont successivement ou en même
temps en contact thermique avec le système.
Lentropie échangée est : 
- Cas dune transformation réversible
Dans une transformation réversible, le système passe par une
suite continue détats déquilibre. Pour sapprocher de cette
condition, il convient quà chaque instant linteraction avec lextérieur
modifie faiblement létat déquilibre existant. Les échanges
de chaleur entre système et sources devront être "peu importants",
donc les températures du système et des sources voisines (notre
sens commun, à défaut de nos connaissances sur le transfert
thermique, nous persuade que les échanges de chaleur augmente avec
les différences de températures).
Dans le cas idéal de la transformation réversible, les températures
du système et des sources sont identiques.
Cette relation, égalité des températures entre système
et milieu extérieur, traduit la condition déquilibre
pour un système en interaction thermique.
Si, entre les instants t et t + dt, d
Q est la quantité de chaleur échangée avec
la (les) source(s), T la température commune, alors d
Se = d Q
/ T.
Comme Sc = 0, on obtient 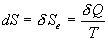 ,
ou en intégrant
,
ou en intégrant 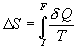 .
.
Remarque : lunité légale de mesure de lentropie est le
Joule/Kelvin (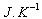 ).
).
1.2. Entropie dun système isolé
fermé
Un système isolé hors déquilibre évolue
vers un état déquilibre " naturel ou non-contraint ", cest
à dire vers un état déquilibre qui nest pas imposé
par laction du milieu extérieur.
Lécriture du second principe montre que lentropie est maximale
puisque celle-ci augmente pendant lévolution vers létat
déquilibre.
Ce résultat, à savoir lexistence dune fonction dont
la valeur est extrémale à léquilibre est dune
portée générale en Physique.
Deux fois déjà, dans vos études, cette notion
a été abordée :
- en Optique géométrique où vous avez appris que,
suivant le Principe de Fermat, le chemin optique est extrémal, cest
à dire que le temps mis par la lumière dans le sens de propagation
pour aller dun point à un autre est minimal,
- en Mécanique où, pour un équilibre stable cest
à dire naturel, lénergie potentielle est minimale.
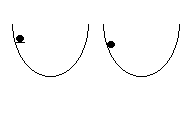 |
Lexemple ci-contre nous aide à mieux
comprendre. Dans la cuvette de gauche, il y a un taquet et la bille est
en équilibre contraint. Dans la cuvette de droite, il ny a pas
de taquet et la position déquilibre naturel de la bille est la
position la plus basse où son énergie potentielle est moindre
que dans léquilibre contraint. |
On remarquera que, sans frottement cest à dire sans perte dénergie
mécanique, la bille ne se stabilisera pas à sa position déquilibre
naturel.
1.3. Remarques
-
lutilisation de fonctions extrémales à léquilibre
(et leur définition suivant les conditions de l'équilibre)
est importante en Thermodynamique ; néanmoins, nous estimons que
leur introduction dans ce cours serait trop ambitieuse pour un " premier
contact " avec cette matière.
-
on entend et on lit, parfois sans justificatifs, beaucoup de choses sur
lentropie, par exemple :
- lentropie de lUnivers croît ce qui entraînerait sa
mort thermique,
- lentropie est une mesure du désordre.
La démarche scientifique implique de la rigueur et le professeur
doit se donner les moyens pour expliquer, pour faire comprendre sachant
parfaitement que tout ne sera pas assimilé ... sinon il vaut mieux
savoir dire que certaines questions ne peuvent être exigées,
sont dun niveau supérieur.
Nous traiterons de cas " en attente " le premier exemple.
Le second exemple est fondamental en Physique mais, pour aborder
cette question, il faut des connaissances certaines de Thermodynamique
statistique, il faut être capable de comprendre ce quest un état
quantique, être capable de compter les états microscopiques
correspondant à un même état macroscopique, ... : dans
le cadre de lenseignement de la Physique en DEUG A, la commission des
programmes estime que cet enseignement est difficile et quil convient
dattendre le 2ème cycle, cest à dire le niveau
licence.
1.4. Conséquences mathématiques des
premier et second principes
Nous avons introduit deux fonctions détat U et S (trois
avec lenthalpie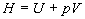 mais cette dernière se déduit directement de U ou inversement)
, leurs variations sont indépendantes de la transformation et ne dépendent
que des états initial et final.
mais cette dernière se déduit directement de U ou inversement)
, leurs variations sont indépendantes de la transformation et ne dépendent
que des états initial et final.
Nous disposons de deux méthodes pour calculer ces variations,
- connaître une transformation quelconque entre état initial
et état final et faire le calcul,
- connaître les fonctions détat et exprimer leurs variations.
Connaissance de U (ou H) et S
Nous apprendrons que les formes différentielles d
W
+ d
Q et dQ/
T dun système sont connues.
Ces formes différentielles sont respectivement, selon les premier
et second principes, les différentielles dU et dS
des fonctions U et S.
Les Mathématiques nous apprennent que des formes différentielles
de ce type sont des différentielles totales exactes qui possèdent
des propriétés remarquables, en particulier celle dobéir
au critère de Cauchy.
Le lecteur intéressé par laspect mathématique
de la Thermodynamique peut, dès à présent, se reporter
au chapitre 7 " Propriétés de la matière " en sappuyant
sur lannexe " Eléments de Mathématiques " en fin du polycopié.
Calcul de Sc
Ce calcul ne peut être fait quà partir de 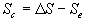 .
.
2. Les énoncés historiques
de Clausius et Thomson
2.1. Enoncé de Clausius
" La chaleur ne passe pas spontanément dun corps froid sur un
corps chaud "
Considérons un système 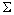 isolé
thermiquement constitué de deux sous-systèmes
isolé
thermiquement constitué de deux sous-systèmes  et
et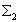 de températures
respectives
de températures
respectives 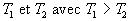 échangeant entre eux uniquement de lénergie thermique.
échangeant entre eux uniquement de lénergie thermique.
Nous nous plaçons entre les instants t et 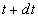 où nous pouvons considérer
où nous pouvons considérer 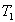 et
et 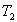 fixées,
nous notons
fixées,
nous notons 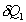 et
et 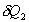 les échanges
de chaleur respectivement aux systèmes
les échanges
de chaleur respectivement aux systèmes  et
et 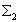 .
.
Lisolation thermique de 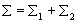 conduit à
conduit à  et à
et à 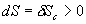 puisque le système
puisque le système 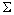 néchange pas de chaleur.
néchange pas de chaleur.
Le caractère additif de lentropie permet décrire aussi 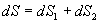
Le calcul de 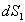 ou
ou 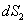 ne nécessite
pas de connaître la transformation, il convient de respecter état
initial et état final.
ne nécessite
pas de connaître la transformation, il convient de respecter état
initial et état final.
Ainsi pour le système 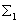 (ou
(ou 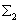 ) à
température
) à
température (ou
(ou  ), nous
pouvons imaginer quil a échangé
), nous
pouvons imaginer quil a échangé 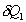 (ou
(ou 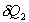 ) dans
une transformation réversible cest à dire avec une source à
température
) dans
une transformation réversible cest à dire avec une source à
température  (ou
(ou  ).
).
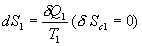 et
et 
Soit 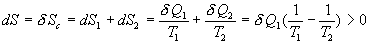
ce qui entraîne 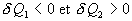 .
.
La chaleur passe spontanément du corps chaud sur le corps
froid.
Remarque : nous aurions pu raisonner à partir du seul système 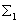 (ou du seul système
(ou du seul système 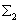 )
et nous aurions trouvé, évidemment, des résultats identiques
; par contre nous ne sommes pas capable daffecter lentropie créée
par irréversibilité, lexercice du mur (voir ci-après dans
le paragraphe 3) montre que cette entropie dirréversibilité est
principalement créée dans le système " séparant
" les systèmes
)
et nous aurions trouvé, évidemment, des résultats identiques
; par contre nous ne sommes pas capable daffecter lentropie créée
par irréversibilité, lexercice du mur (voir ci-après dans
le paragraphe 3) montre que cette entropie dirréversibilité est
principalement créée dans le système " séparant
" les systèmes 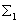 et
et 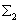 .
.
2.2. Enoncé de Thomson
" Un système en contact avec une seule source de chaleur ne peut,
au cours dun cycle, que recevoir du travail et fournir de la chaleur "
Le premier principe sécrit 0 = W + Q
Le second principe sécrit 0 = Q / TS
+ Sc ce qui entraîne 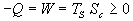
Généralement, on exprime ce résultat par la phrase :
"avec une seule source de chaleur, on ne peut réaliser une machine
thermique motrice".
3. Les causes dirréversibilité
Exemple dirréversibilité : le transfert thermique
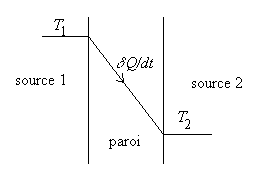 |
Une source de chaleur 1 à température
constante T1 fournit de la chaleur
à une source de chaleur 2 à température constante
T2
(T1 > T2
). Le contact thermique est assuré par une simple paroi solide.
Si les deux sources sont des fluides nous sommes dans le cas dun échangeur.
Nous nous situons en régime permanent et considérons
comme système la paroi. Ce système est en état de
déséquilibre, cependant les variables détat gardent
des valeurs constantes en chaque point. |
Par suite la variation dentropie au cours du temps sera nulle (DS
= 0). Le système échange de la chaleur, donc de lentropie,
avec chacune des sources. Il reçoit, par unité de temps,
lénergie calorifique dQ / dt
de la part de la source à température T1
quil perd avec celle à température T2
.
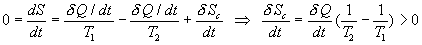
Le transfert thermique qui a lieu spontanément des parties
chaudes vers les parties froides est une cause importante dirréversibilité.
Les causes dirréversibilité
-
En labsence de champs extérieurs, la non-uniformité de grandeurs
telles que la densité des particules, la pression, la température,
... sont des causes dirréversibilité
-
Les travaux des forces qui se transforment systématiquement en énergie
interne et/ou en chaleur sont des causes dirréversibilité.
Il sagit de forces de frottement visqueux, ou solide, deffet joule, de
" frottement chimique ".
Souvent une notion de " lenteur ou de non-brutalité " est
associée aux transformations réversibles.
Léchelle de temps peut être très différente
suivant la cause dirréversibilité. Ainsi les phénomènes
où les gradients de température sont cause dirréversibilité
sont particulièrement lents par rapport à ceux où
sont impliqués les gradients de pression.
Annexe : quelques rappels simples
de Mécanique
1. Chute libre
Dans un référentiel galiléen dorigine O daxe vertical
ascendant Oz, létude de la chute libre dun corps " ponctuel " M de
masse m (en première approximation, il sagit dun référentiel
lié au sol, de la chute dun corps suffisamment dense et de la vitesse 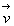 de son centre de masse) conduit à
de son centre de masse) conduit à  cest à dire à la conversation de cette quantité au cours
du mouvement (g est lintensité du champ de pesanteur).
cest à dire à la conversation de cette quantité au cours
du mouvement (g est lintensité du champ de pesanteur).
Linterprétation donnée à ce résultat à
partir du principe fondamental de la dynamique est la suivante :
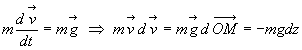 ; par intégration
; par intégration 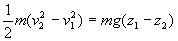
ou encore 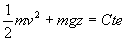
Par définition, 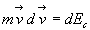 est la différentielle de lénergie cinétique dune masse
ponctuelle,
est la différentielle de lénergie cinétique dune masse
ponctuelle, 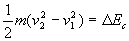 la variation de lénergie cinétique et
la variation de lénergie cinétique et 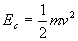 lénergie cinétique.
lénergie cinétique.
Les forces de pesanteur sont un cas très particulier. Le travail élémentaire
dune force est défini, de manière tout à fait générale,
par la relation 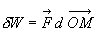 qui, pour la force de pesanteur, devient
qui, pour la force de pesanteur, devient 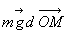 .
.
Lintégration dun point M1 à
un point M2 conduit à 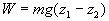 ,
le travail est indépendant de la trajectoire, il ne dépend que
de la différence daltitude, des points de départ et darrivée.
,
le travail est indépendant de la trajectoire, il ne dépend que
de la différence daltitude, des points de départ et darrivée.
2. Théorème de lénergie cinétique
Lénergie cinétique se généralise à un ensemble
matériel constituant un système (déformable ou non) et
le théorème de lénergie cinétique sécrit
: 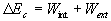 où
Wint est le travail des forces intérieures
au système et Wext le travail des forces
extérieures sappliquant sur le système.
où
Wint est le travail des forces intérieures
au système et Wext le travail des forces
extérieures sappliquant sur le système.
3. Forces dérivant dune fonction potentielle (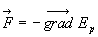 ).
Forces conservatives
).
Forces conservatives
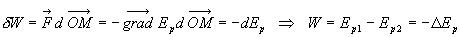 (le travail
est indépendant de la trajectoire, il ne dépend que des points
initial et final).
(le travail
est indépendant de la trajectoire, il ne dépend que des points
initial et final).
Le théorème de lénergie cinétique peut être
réécrit ainsi 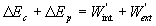 où
Wint et Wext
sont les travaux des forces intérieures et extérieures ne dérivant
pas dun potentiel.
où
Wint et Wext
sont les travaux des forces intérieures et extérieures ne dérivant
pas dun potentiel.
Sil nexiste que des forces dérivant dun potentiel, alors 
Les forces dérivant dun potentiel sont appelées forces conservatives
car, au cours du mouvement, elles conservent la quantité 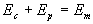 .
.
Ep est appelée énergie
potentielle et Eménergie
mécanique.
Remarque : pour la force de pesanteur, on montrera, sans peine, que 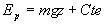
4. Signification des termes " énergie cinétique
" et " énergie potentielle "
Le mot énergie vient du grec energhia
qui signifie " force en action " cest à dire capacité à
produire un mouvement.
Ainsi un corps qui possède de lénergie cinétique
(jadis appelée " force vive ") peut continuer, de lui-même,
son mouvement au moins sur une certaine distance même dans un milieu
résistant (sopposant au mouvement).
En quoi lénergie potentielle (jadis appelée "
force morte ") a telle cette capacité à produire un mouvement
?
Reprenons lexemple de la chute libre. Un corps immobile, non tenu
à une altitude z, spontanément chute et acquiert de lénergie
cinétique. Il a donc, en lui, une capacité à produire
un mouvement, il a une énergie que nous appelons potentielle cest
à dire susceptible dêtre produite.
5. Forces non conservatives
5.1. Forces dopérateur extérieur
Comment le corps a til acquis cette énergie potentielle de pesanteur
? Il nest pas venu à laltitude z spontanément, il a fallu
un opérateur extérieur pour exercer sur le corps une force
opposée au poids du corps. Pour un corps ponctuel,
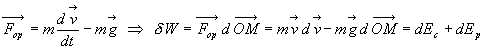
Le travail de la force produite par lopérateur extérieur
est transformé en énergie cinétique et énergie
potentielle.
Le travail de lopérateur extérieur nest pas perdu,
il a servi à augmenter lénergie cinétique et potentielle
du corps.
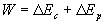
Le travail de lopérateur extérieur na pas un caractère
conservatif puisque la quantité 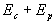 nest
pas conservée. Il sagit dune force non conservative.
nest
pas conservée. Il sagit dune force non conservative.
Le travail des forces non conservatives doit être compris comme
un échange dénergie entre deux systèmes. En
aucun cas, il ne peut être considéré comme une énergie
de lun ou de lautre des systèmes.
Remarque : Si lintensité de cette force est très
légèrement supérieure à celle du poids, alors
le corps est porté à laltitude z à vitesse pratiquement
nulle (en Thermodynamique, on parle dun mouvement fait dune succession
détats déquilibre) et le travail de lopérateur,
qui est minimal dans ce cas, est transformé uniquement en énergie
potentielle.
5.2. Forces de frottement
Nous envisageons la chute dun corps dans un milieu résistant
(exemple le parachute).
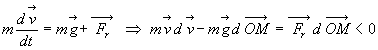 puisqu' une force
résistante soppose au mouvement.
puisqu' une force
résistante soppose au mouvement.
En conséquence, 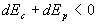 , lénergie mécanique diminue, elle nest pas conservée.
, lénergie mécanique diminue, elle nest pas conservée.
Il y a perte dénergie mécanique. Le corps perd de son
énergie mécanique pour se mouvoir malgré la force
résistante.

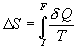 .
.

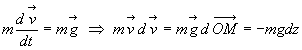 ; par intégration
; par intégration 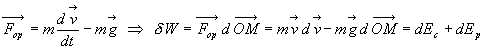
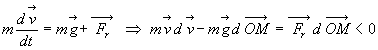 puisqu' une force
résistante soppose au mouvement.
puisqu' une force
résistante soppose au mouvement.